Суть продукта, обзор характеристики:
Обзор: Хлорид аммония Ядовитый газ который применяется в жизни человека.
Химия. Хлорид аммония
Описание.
Сегодня поговорим о химии, наш гость хлорид аммония который знаком ещё со школьным уроком по химии, он представляет из себя порошок мелко кристаллического белого цвета, отлично растворяется в H20, гидролизуется и легко сдувается.
Характеристики основные! Молярная масса 54 грамм на моль, растворимость в воде 37.2, молекулярная формула NH4CL.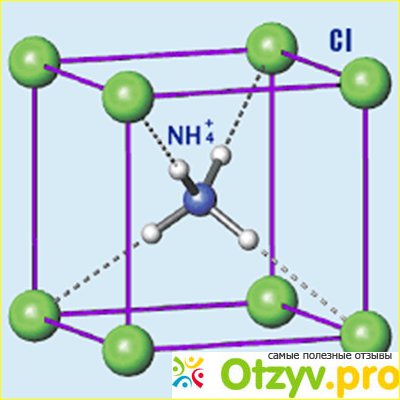
Описание элемента.
Является, бесцветный ядовитый газ с резким запахом, который легко растворим в H2O, может переходить в бесцветную жидкость, и в твердое состояние. Водный раствор называют соляной кислотой. Соляная кислота взаимодействуют со всеми металлами, в природе распространены и применяются в нуждах человека.
Например хлорка для бассейна которая убивают все бактерии. Хлорки которые уборщицы применяют для того чтобы уничтожить всю грязь и бактерии. Сильный запах, при длительном контакте у человека начинают чесаться глаза, идут слезы. Также вредно для здоровью способно убить человека.
Способ получения.
Для того чтобы это изготовить надо, вещества, колбы, применяется в промышленности, некогда не экспериментировал, получить можно в домашних условиях, и на уроке. Такую соль получается из отделения NaHCO3.
Формула получения на промышленности (nacl+h2o+co2+nh3=nahco3+nh4cl).
8nh3+3cl2=6nh4cl+n2. nh3+hcl=nh4cl.
Получается в слабом нагревание благодаря H2SO4, хлорида натрия.
Химические свойства.
Это соль со слабым основанием, с помощью хлороводородной все это в растворе гидролизуется, при нагревание наш аммоний разлагается на аммиак, и хлороводород, которые через несколько время вновь соединяется. Реагирует с оксидами, металлами, хлором. На все это есть формулы чтобы лучше узнать как происходит процесс надо записать формулы.
Применение в химии.
Применяется в красильном деле, хорошо взаимодействует с металлами таким образом прилипает к нему, при прикосновение к нагретому металлу, может случится два варианта! Либо восстановиться или станет хлоридом.
В жизни человека.
В жизни человека играют важную роль! Как и говорил при уборке чтобы уничтожить инфекции и прочую нечистую силу, обработку руд, очистка сосудов, в строительных материалов. Например плита тротуара, железобетонные изделия.
Опасен?
Да, является ядовитым газом, вдыхание приводит кашель, удушение, заложен нос, в тяжелых случаях может возникнуть оттек легких, может привести к смерти.
Видео обзор
| Все(5) |
|---|
 Химия из батарейки - Хлорид аммония - Хлорид олова(II) реактив на ионы золота Химия из батарейки - Хлорид аммония - Хлорид олова(II) реактив на ионы золота |  Получение хлорида аммония Получение хлорида аммония |  хлорид аммония хлорид аммония |  Прикольные химические реакции, дым без огня, получение ( синтез ) хлорида аммония NH4Cl Прикольные химические реакции, дым без огня, получение ( синтез ) хлорида аммония NH4Cl |  хлорид аммония с гидроксидом хлорид аммония с гидроксидом |






Комментарии на отзыв: